Хворому на Паркінсона вперше пересадили нейрони, отримані з його власних клітин шкіри
Експеримент тримали в секреті, проте він виявився абсолютно легальним і безпечним. З моменту операції минуло два з половиною роки, за цей час ніяких побічних ефектів не з'явилося. А стан хворого стабілізувався — про прогрес говорити рано, але й ознак нейродегенерації лікарі не виявили. Дослідження опубліковане в журналі The New England Journal of Medicine.
Технологія клітинного репрограмування з'явилася ще в 2006 році, але її клінічних застосувань дотепер не так багато. Річ у тому, що сам процес — перетворення дорослих клітин в індуковані плюрипотентні клітини (аналог ембріональних стовбурових), — поки проходить з низькою ефективністю. Крім того, ембріональні клітини здатні утворювати пухлини, і навіть після того, як їх диференціюють в якийсь конкретний тип клітин, в культурі можуть залишатися небезпечні клони. Тому поки терапії з використанням репрограмування зустрічаються рідко. Наприклад, восени 2019 року через репрограмування клітин вперше виростили роговицю, а на початку 2020 року — «латочку» для серця.
В обох випадках першопрохідцями стали японські дослідники — відтоді, як японські ж біологи придумали репрограмувати дорослі клітини в стовбурові, ця країна стала однією з лідерів в галузі клітинної терапії. У 2018 році в Японії з'явився проєкт ще одного методу: вчені зібралися випробувати репрограмування проти хвороби Паркінсона, тобто перетворити дорослі клітини в ембріональні, виростити з них клітини-попередники нейронів і підсадити в мозок пацієнта. Клінічні випробування стартували восени 2018 року, але їх результати ще не опубліковані.
Японська команда була першою, хто заговорив про подібний експерименті, але, як виявилося, не першою, хто його запустив. Як з'ясував журнал STAT, в США подібний план дозрівав з 2014 року. У 2017 році, коли в Японії тільки планували випробування, перший пацієнт уже отримав ін'єкцію клітин, а тепер команда медиків під керівництвом Кван Су Кіма (Kwang-Soo Kim) з лікарні Маклін в Массачусетсі опублікувала звіт про цю експериментальну терапію.
За даними STAT, перший пацієнт — американський бізнесмен, колишній лікар Джордж Лопес — знайшов Кіма сам у 2013 році і запропонував проспонсорувати його дослідження. На той час Лопес вже знав, що у нього хвороба Паркінсона, але не розраховував на те, що лікарі зможуть йому допомогти. Проте, отримавши фінансування і прискоривши дослідження, через кілька років Кім вже був готовий випробувати на Лопесі свій метод.
Дослідники взяли людські клітини шкіри, репрограмували їх в ембріональні стовбурові, а потім диференціювали в попередники дофамінергічних нейронів — тих самих, які гинуть у пацієнтів з хворобою Паркінсона. Щоб переконатися в тому, що їх протокол надійний, Кім і колеги перевіряли його на гуманізованих мишах — це тварини з імунодефіцитом, яким пересаджують людські клітини крові. Їм імплантували отримані нейрони в мозок, а потім стежили за рівнем імунної агресії. Як і слід було очікувати, якщо клітини крові і нейрони були отримані від одного пацієнта, імунної відповіді не виникало, а якщо від різних, в мозку розвивалося запалення.
Водночас автори роботи придумали спосіб позбутися недиференційованих клітин в культурі. Для цього їх обробляли кверцетином — це речовина рослинного походження, яку використовують в протипухлинній терапії — після чого «підозрілих» клітин залишилося не більше однієї на мільярд.
Кім і колеги тримали свій експеримент в таємниці і не публікували попередніх заяв. Однак, він був абсолютно легальним: вони отримали дозвіл від FDA на застосування свого методу у виняткових обставинах — тобто тільки у невиліковно хворої людини, причому кожен раз процедуру необхідно погоджувати заново. На першому етапі роботи FDA погодило введення клітин тільки в ліву півкулю мозку. На другу серію ін'єкцій — в праву півкулю — відомство погодилося тільки через пів року, коли стало зрозуміло, що процедура не викликає побічних ефектів.
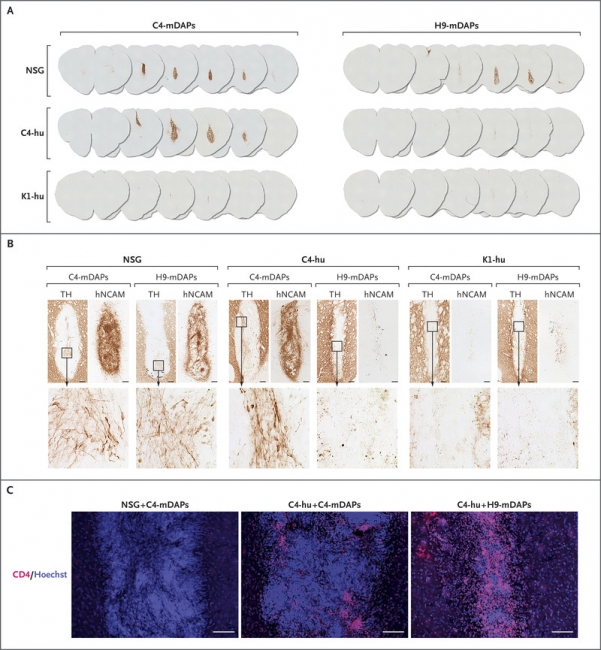
Імуногенність нейронів в мозку миші. Зліва направо: імунодефіцитні миші після пересадки нейронів, імунодефіцитні миші після трансплантації клітин крові і нейронів від одного донора, імунодефіцитні миші після трансплантації клітин крові і нейронів від різних донорів. Синій — ядра клітин, червоний — лімфоцити, ознака запалення.
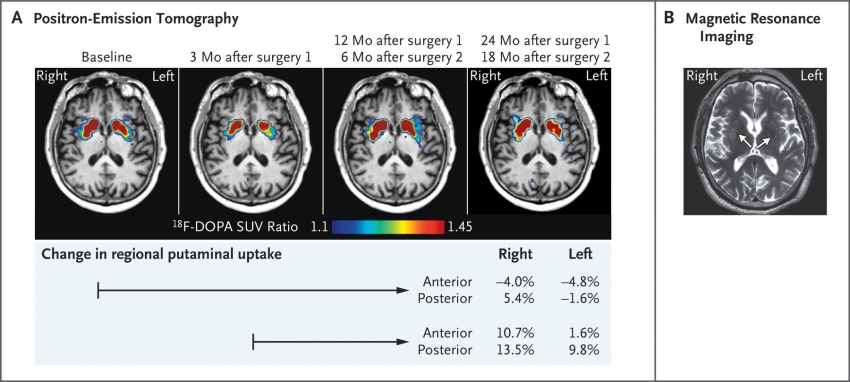
За станом Лопеса лікарі стежили за допомогою МРТ, в тому числі з використанням міченої амінокислоти-попередника дофаміну. Чим більше нейрони поглинають цієї речовини, тим більше вони виробляють дофаміну, отже, тим слабкіше нейродегенерація. Судячи з МРТ, ніяких новоутворень в мозку Лопеса за два роки не виникло, а нейрони стали захоплювати трохи більше амінокислот, ніж раніше.
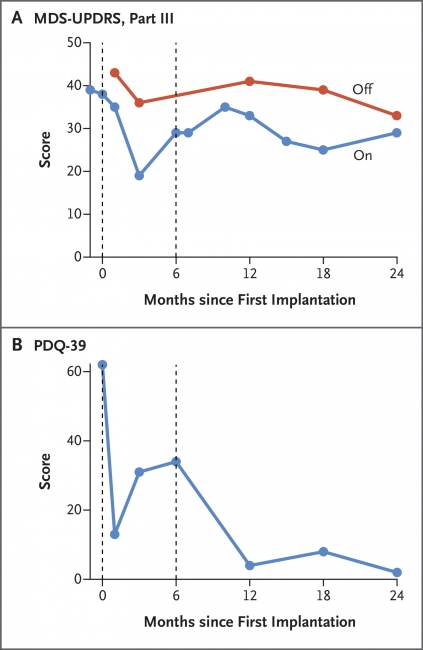
Функціональний стан пацієнта дослідники оцінювали за двома шкалами: одна відповідала за моторні навички, друга — за якість життя. За час експерименту моторні навички змінилися неістотно, тому автори роботи визнали, що нейродегенерація в його мозку призупинилася. Якість життя ж покращилося значно, проте дослідники відзначають, що ця оцінка суб'єктивна. Сам же пацієнт помітив, що кількість «викинутих годин», коли він не здатний працювати й координувати свої рухи, знизилася від трьох до однієї години в день. Він продовжує приймати ті ж ліки, що і до операції — це стандартна терапія при хворобі Паркінсона, і необхідна доза за час спостереження знизилася несуттєво, всього на шість відсотків.
Кім і колеги продовжують спостереження за станом Лопеса. Вони не виключають, що клітинна терапія може в довгостроковій перспективі дати ефект, який поки ще не проявився. Водночас вони відзначають, що про зцілення від хвороби мова поки не йде, тільки про стабілізацію стану. Крім того, вони звертають увагу на те, що Лопесу не знадобилася імуносупресія — це підтверджує безпеку використання власних репрограмованих клітин пацієнта.